





食品安全国家标准 食品添加剂 稳定态二氧化氯溶
2013-08-15
1 范围
本标准适用于经食品添加剂碳酸盐吸收二氧化氯气体制得的食品添加剂稳定态二氧化氯溶液。该产品在使用时用食品添加剂盐酸进行活化。
2 规范性引用文件
本标准中引用的文件对于本标准的应用是必不可少的。凡是注日期的引用文件,仅所注日期的版本适用于本标准。凡是不注日期的引用文件,其最新版本(包括所有的修改单)适用于本标准。
3 技术要求
3.1感官要求:应符合表1 的规定。
表1感官要求
|
项目 |
要求 |
检验方法 |
|
色泽 |
无色或黄色。 |
取适量试样置于比色管中,在自然光下观察色泽和组织状态。 |
|
组织状态 |
透明液体,无悬浮物。 |
3.2理化指标:应符合表2的规定。
表2理化指标
|
项目 |
指 标 |
检验方法 |
|
二氧化氯,w/%≥ |
2.0 |
附录A中A.4 |
|
密度,ρ20/(g/mL) |
1.020~1.060 |
附录A中A.5 |
|
pH |
8.2~9.2 |
附录A中A.6 |
|
砷(As)/(mg/kg)≤ |
1 |
附录A中A.7 |
|
重金属(以Pb计)/(mg/kg)≤ |
5 |
附录A中A.8 |
|
甲醇,ρ/(g/100mL)≤ |
0.04 |
附录A中A.9 |
A.1 警示
附 录 A
(规范性附录)
检验方法
本标准的检验方法中使用的部分试剂具有腐蚀性,操作者须小心谨慎!如溅到皮肤上应立即用水冲洗,严重者应立即就医。使用易燃品时,严禁使用明火加热。
A.2 一般规定
本标准的检验方法中所用试剂和水,在没有注明其他要求时,均指分析纯试剂和GB/T 6682—2008中规定的三级水。试验中所用标准滴定溶液、杂质标准溶液、制剂及制品,在没有注明其他要求时,均按HG/T 3696.1、HG/T 3696.2、HG/T 3696.3之规定制备。
A.3 鉴别试验
用盐酸浸润的铂丝先在无色火焰上燃烧至无色。再蘸取少许试验溶液,在无色火焰上燃烧,通过钴玻璃观察火焰呈鲜黄色。
在试液中加入氯化钙溶液,产生白色沉淀。该沉淀溶于盐酸中。
在试液中加盐酸溶液后可产生黄色气体,同时试液也呈黄色。
A.4 二氧化氯含量的测定
第一步在pH≤2时,用丙二酸掩蔽次氯酸根(即氯气)的干扰,样品中的二氧化氯和全部的亚氯酸根与碘化钾反应,用硫代硫酸钠标准溶液滴定生成的碘。第二步取另一份样品,调节溶液pH≤2,用氮气赶去二氧化氯和氯气,样品中的亚氯酸根与碘化钾反应,用硫代硫酸钠标准溶液滴定生成的碘。通过两步反应之差计算出样品中二氧化氯的实际含量。
称取约10 g试样,精确至0.000 2 g,转移至50mL容量瓶中,用水稀释至刻度,摇匀。该溶液为试验溶液A,用于二氧化氯含量的测定。
用移液管分别移取10.00mL试验溶液A,置于两个已预先加入50mL水的碘量瓶中,分别加入2mL盐酸溶液,加盖水封放置30min后立即按第一步和第二步进行测定。
第一步:在一个碘量瓶中加入3 mL丙二酸溶液,置于暗处静置3 min。加入10 mL硫酸溶液,10 mL碘化钾溶液,混匀,置于暗处静置5 min。用硫代硫酸钠标准滴定溶液滴定,近终点时加入1 mL淀粉指示液,继续滴定至蓝色刚好消失为终点,记录消耗的体积为V1。
第二步:将另一个碘量瓶置于通风良好的通风橱内,通入高纯氮气吹至黄绿色消失后再吹20 min。加入3 mL丙二酸溶液,置于暗处静置3 min。加入10 mL硫酸溶液,10 mL碘化钾溶液,混匀,置于暗处静置5 min。用硫代硫酸钠标准滴定溶液滴定,近终点时加入1 mL淀粉指示液,继续滴至蓝色刚好消失为终点,记录消耗的体积为V2。
二氧化氯含量以二氧化氯(ClO2)的质量分数w1计,数值以%表示,按公式(A.1)计算:
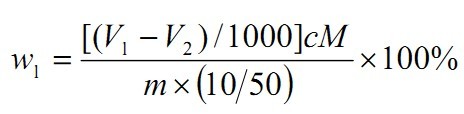
式中:
V1——第一步滴定试验溶液消耗硫代硫酸钠标准滴定溶液体积的数值,单位为毫升(mL);
V2——第二步滴定试验溶液消耗硫代硫酸钠标准滴定溶液体积的数值,单位为毫升(mL);
c ——硫代硫酸钠标准滴定溶液浓度的准确数值,单位为摩尔每升(mol/L);
m——试料的质量的数值,单位为克(g);
M——二氧化氯(1/5ClO2)摩尔质量的数值,单位为克每摩尔(g/mol)(M=13.49)。
取平行测定结果的算术平均值为测定结果,两次平行测定结果的绝对差值不大于0.02%。
二氧化氯在430nm处有特征吸收,使用分光光度法进行测定。
在水中加入亚硫酸钠,以DPD余氯测定试剂检查不显色,再进行蒸馏,收集馏出液。
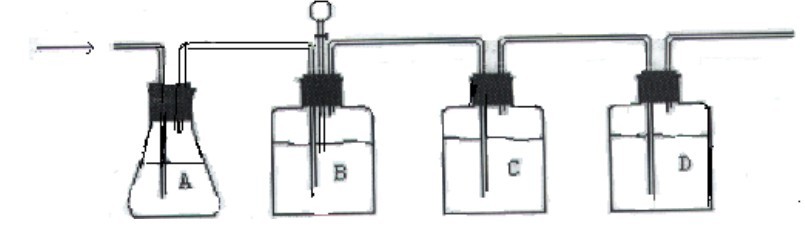
制备:在A瓶中放入300 mL水,将A瓶一端玻璃管与空气压缩机相接,另一玻璃管与B瓶相连。B瓶为高强度硼硅玻璃瓶,瓶口有三根玻璃管;第一根插至离玻璃瓶底5 mm处,用以引进空气;第二根上接滴液漏斗,漏斗下端伸至液面下;第三根下端离开液面,上端与C瓶相接。溶解10 g亚氯酸钠于750 mL水中并倒入B瓶中;在分液漏斗中装有1+10硫酸溶液20 mL。C瓶装有亚氯酸钠饱和溶液。D瓶为2 L硼硅玻璃收集瓶,瓶中装有1500 mL水,用以吸收所发生的二氧化氯,余气由排气管排出。整套装置应放在通风橱内 (见图A.1)。
|
−3 |
|
m×10 |
启动空气压缩机,使空气均衡通过整个装置。每隔5 min由分液漏斗加入5 mL硫酸溶液,加完最后一次硫酸溶液后,空气流量持续30 min。所获得的黄色二氧化氯标准溶液放于棕色瓶中,4℃下保存,其浓度应为250 mg/L~600 mg/L。
按
根据测定的二氧化氯贮备液的浓度,吸取一定量二氧化氯标准贮备液,用无氯蒸馏水进行稀释。该溶液即用即配。
分别取0.00 mL、10.00 mL、20.00 mL、40.00 mL、60.00 mL、80.00 mL、100.00 mL二氧化氯标准溶液,置于七个100 mL容量瓶中,用无氯蒸馏水稀释至刻度,摇匀。在430 nm波长下,选用1 cm比色皿,以无氯蒸馏水调零,测量吸光度。
从每个标准溶液的吸光度中减去试剂空白溶液的吸光度,以二氧化氯的质量(mg)为横坐标,对应吸光度为纵坐标,绘制工作曲线。
称取0.7 g试样,精确至0.000 2 g,加入10 mL盐酸溶液,转移至100 mL容量瓶中,用无氯蒸馏水稀释至刻度,摇匀。在430 nm波长下,选用1 cm比色皿,以无氯蒸馏水调零,测量吸光度。从工作曲线上查出试验溶液中二氧化氯的质量。
二氧化氯含量以二氧化氯(ClO2)的质量分数w1计,数值以%表示,按公式(A.2)计算:
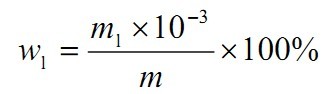
式中:
m1——从工作曲线上查得的试验溶液中二氧化氯的质量的数值,单位为毫克(mg);
m ——试料的质量的数值,单位为克(g)。
取平行测定结果的算术平均值为测定结果,平行测定结果的绝对差值不大于0.02%。
同GB/T 4472-1984中
同GB/T 4472-1984中
取平行测定结果的算术平均值为测定结果,两次平行测定结果的绝对差值不大于0.003 g/cm。
A.6 pH的测定
同GB/T 9724-2007的第5章。
将试样倒入烧杯中,以下按GB/T 9724-2007的第6章测定。
取平行测定结果的算术平均值为测定结果,两次平行测定结果的绝对差值不大于0.2 pH单位。
A.7 砷的测定
称取1.00 g±0.01 g试样,置于100mL烧杯中,加盐酸溶液(1+3)8 mL。置于电炉上煮沸至近干,取下冷却至室温,加少量水,作为试验溶液。
限量标准溶液的配制:移取1.00 mL砷标准溶液[1mL溶液含1.0μg砷(As)],以下按GB/T 5009.76-2003的第11章操作,从“分别置于锥形瓶中……”开始测定。
A.8 重金属的测定
称取1.00 g±0.01 g试样,置于100 mL烧杯中,加入盐酸溶液(1+3)8mL,置于电炉上煮沸至近干,取下冷却至室温,加少量水,移入50 mL比色管中,加入1滴酚酞指示液,用氨水溶液和盐酸溶液调节溶液的pH值为中性(酚酞红色刚褪去)作为试验溶液。
用移液管移取0.50mL铅标准溶液[1 mL溶液含0.01mg铅(Pb)]作为标准,以下按GB/T 5009.74-2003
第6章进行测定。
A.9 甲醇的测定
称取3 g高锰酸钾,加入15 mL磷酸与70 mL水的混合液中,溶解后加水至100 mL。贮存于棕色瓶内。
称取5 g无水草酸或7 g含2个结晶水的草酸,用1+1硫酸溶液溶解并稀释至100 mL。
称取0.1 g碱性品红研细后,分次加入80 ℃的水共60 mL,边加水边研磨使其溶解,用滴管吸取上层溶液滤于100 mL容量瓶中。冷却后加100 g/L亚硫酸钠溶液10 mL,加1 mL盐酸,再加水至刻度,充分混匀,放置过夜。如溶液有颜色,可加少量活性炭搅拌后过滤,贮于棕色瓶中,置暗处保存,溶液呈红色时应重新配制。
称取1.000 g甲醇,置于100 mL容量瓶中,加水稀释至刻度,摇匀。
用移液管移取10.00 mL甲醇标准贮备溶液(
用移液管移取1.00 mL试样,置于25 mL具塞比色管中,加水至15 mL,作为试验溶液。
限量标准溶液的配制:移取0.40 mL甲醇标准溶液(
在两个比色管中分别加入2 mL高锰酸钾-磷酸溶液,混匀,放置10 min。加入2 mL草酸-硫酸溶液,混匀使之褪色,再加入5 mL品红-亚硫酸溶液,用水稀释至刻度,摇匀。于20 ℃以上静置30 min,试样所呈颜色不得深于标准。